
滴眼給藥毒性試驗1-目的與試驗(yàn)設(shè)計
滴眼給藥毒性試驗的目(mù)的
滴眼給藥毒性試驗是重複給(gěi)藥一般毒性試驗,主要用於研發滴(dī)眼藥物。歐盟發(fā)布的《醫療用品非臨床局部(bù)耐受性試驗指導原則》(CPMP/SWP, 2001)明確規定了單次給藥和重複給藥眼部耐受性試驗的相關事宜。美國食品藥品監督管理(lǐ)局發布的《藥品以及可替代(dài)性給藥藥品非臨床安全性評價指導原(yuán)則(zé)草案》(FDA/CDER, 2008)則明確要求在滴眼給藥時應開展係統藥代動力學(PK)和眼科檢查(包括裂隙(xì)燈顯微鏡檢查、眼底檢查、眼(yǎn)壓測量及組織病理學檢(jiǎn)查)。然而,這兩份指導原則中的相關規定均較簡(jiǎn)要,缺乏滴眼給藥毒性試驗詳細設計的具體內容。目(mù)前,尚無滴(dī)眼給藥毒性試(shì)驗的確(què)切定(dìng)義。日本(衛生福利部,1999)依據(jù)ICH M3指導原則(ICH, 2009)和ICH S4指導原則開展滴眼給藥毒性試驗。這些原(yuán)則(zé)通常適用於係(xì)統給藥的藥物。
有人常常將滴眼給藥毒性試驗與眼(yǎn)刺激試驗混為一談。實際上,滴眼毒(dú)性預試驗(yàn)、一周或兩周的重複給藥滴眼毒性試驗的方案與眼(yǎn)刺激(jī)試驗(yàn)的方案有相似之處(OECD, 2012)。
目前,眼刺激試驗通常(cháng)使用兔子進行,以評估化學物質在粘膜給藥或人(rén)體偶然接觸時的安全性(OECD, 2012)。眼刺(cì)激(jī)試驗的主要目的是檢測眼表的刺激或腐蝕反(fǎn)應。
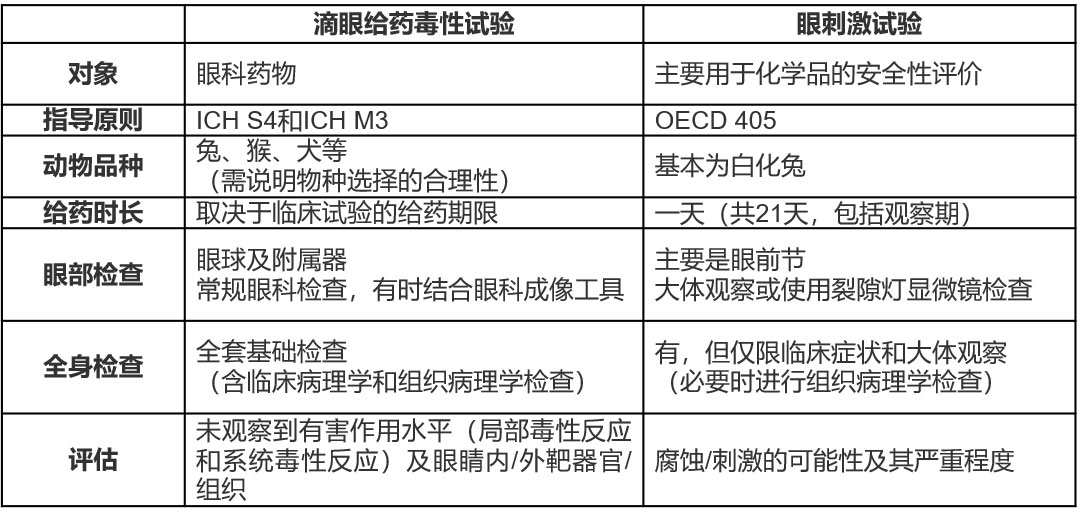
相(xiàng)比之下,滴眼給藥毒性試驗的主要目的是評估眼科藥物的一(yī)般毒性。因此,滴眼給(gěi)藥(yào)毒性試驗的檢查項目包括組織病理學(xué)檢查、眼部附屬器以(yǐ)及全(quán)身髒器的評價(jià)。這兩種試驗的差異見表1。
表1 滴眼給藥毒性試驗和眼刺激試驗的差異
滴(dī)眼給藥毒(dú)性試驗的設計
01、動物物種
根據(jù)ICH M3指導原(yuán)則(zé),一般毒性試驗需選擇兩種動物(ICH, 2009)。通常情況下,會從齧齒類動物(如兔(tù)或小鼠)和非齧齒類動物(犬或猴)中各選一(yī)種。然而,在過去十年間(2005~2016),經日本衛生勞動福利部(MHLW)批準,約九成的滴眼液在(zài)研發過(guò)程中(zhōng),將兔作為開展滴(dī)眼給藥毒性試驗的首選實驗物種,其次(cì)常用的(de)實驗物種是猴(幾乎全部是(shì)食蟹猴),再然後(hòu)是犬(見表2)。因此,滴眼給藥毒性試驗通(tōng)常選擇兩種非(fēi)齧齒類動物。不過,動物物種的選擇是(shì)根據具體情況而定的。因此(cǐ),在評估某些藥物時,可能僅使用(yòng)一個物種(比如兔或食蟹猴)。
表2 2005~2016日本(běn)滴眼液滴眼給藥毒性試驗的(de)獲批的動物物種
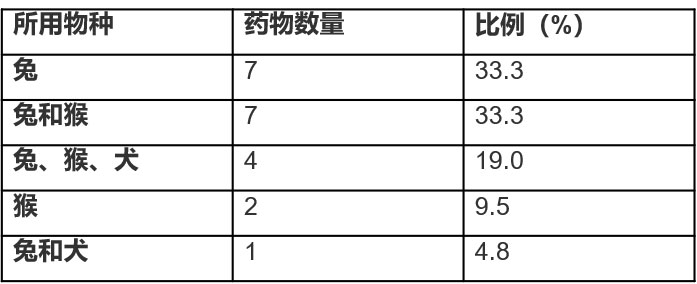
注:信息來源於日本(běn)醫藥和醫療器(qì)械局(PMDA)主頁
近來(lái)發表的多篇(piān)文章從眼部安全性評估(gū)的角度出發,討論了各(gè)個實驗物種的特(tè)點,並(bìng)對(duì)不同(tóng)實驗物種作了比(bǐ)較(jiào)。各(gè)物種的特點如(rú)下(xià)。
兔
兔的(de)眼球重量約為(wéi)人眼的一(yī)半,眨(zhǎ)眼頻率(lǜ)(每6分鍾一次)明顯低於人類的眨眼頻率(每5秒鍾一次)。此外,兔的角膜比人類的角膜薄。基於這些特點,並考(kǎo)慮到(dào)影響藥物角膜滲透能力的因素,有研究者預計,在滴入滴眼液後,兔眼(yǎn)的藥物暴露水平相對(duì)較高。McDonald和Shadduck(1977)認為兔相較於其他實驗動物對眼刺激物更為敏感。使用兔進行試驗的其他原因還包括較(jiào)低的(de)動物成本以及基於大量供試品積累的曆史數據。
在進行滴眼給藥毒(dú)性試驗時,特別需注意選擇色素兔還是白化(huà)兔。由於供試品能夠與色素兔體內的色素結合,因此在毒性評估時(shí),色(sè)素兔更具優勢。關於色素兔,荷(hé)蘭帶兔比新西(xī)蘭大(dà)白兔和新西蘭(lán)紅兔(F1代兔)更常用於滴眼給藥毒性試驗。Durairaj等人(2012)報告稱,人、食蟹猴(hóu)、犬、豬、F1代兔和荷(hé)蘭帶兔的眼部黑色素含量(liàng)存在差異(yì),而且不同物種之間眼睛各部(bù)分的黑色素含(hán)量也不同。另外,值得一(yī)提的是,荷蘭帶(dài)兔的眼球比新西蘭大白兔或日本(běn)白兔的小。
猴(hóu)
盡管食蟹猴的眼球重量僅約為人眼(yǎn)的一半,但其解剖特征與人類相似。例如,食蟹猴的角膜和晶狀(zhuàng)體相對較小,眼底有黃斑。Shibuya等人(2015)建議將(jiāng)食蟹猴用作實驗動物,因為它們的眼睛有助於詳細評估藥(yào)物誘導的黃斑病變毒(dú)性。食蟹猴的(de)眨眼頻率與人類相似。與人(rén)類一樣,食蟹猴既沒有瞬膜(mó),也沒有哈氏腺,而兔、犬和豬則都有瞬膜和哈氏腺。食蟹猴和犬一樣,也用於係統毒性(xìng)試驗。利用(yòng)相關物種可以獲得毒理(lǐ)學數據,彌合局部給藥和係統給藥在同一物種(zhǒng)中產生的結果差異(yì)。與人類相比,食蟹猴的眼組織黑色素含量相對較高。在猴類中(zhōng),視神經退化常見於恒河猴和食蟹猴,且(qiě)被認為是自發性先天視神(shén)經病變。
犬和豬
針對(duì)特定目的飼養的(de)比格犬的眼球(qiú)重量約為5.5克,約為人眼重量的0.8倍,而豬的眼球大小(xiǎo)接近人眼。從(cóng)眼球(qiú)的絕對尺(chǐ)寸來看,犬和豬在藥物局部效(xiào)應評估方麵具有優勢,因為眼組織的厚度和長度是決定局部給藥藥物滲透性(xìng)和分布的重要因素。犬和豬的眼部解剖特征相似,例如,與靈長類動物相比,它們的晶狀體在眼球中占據的體積相對(duì)較大。另一方麵,犬的脈絡膜上有毯(tǎn)氈層,而(ér)豬(zhū)、兔或食蟹猴則沒有。目前,犬和豬不常用於滴眼給藥毒性試驗,尤其是豬。然而,這類動物在滴眼(yǎn)給藥毒(dú)性試驗中仍有其獨特的優勢,理由如下:1. 基於上述解(jiě)剖和生理特點,模仿人(rén)體藥物分布的可能性較高。2. 與兔和食蟹猴相比,由(yóu)於犬和豬的體型相對較大,通過係統給(gěi)藥出現的藥物反(fǎn)應更少。
02、性別
根據一般毒性試驗指導原則(衛生福利部,1999),滴眼(yǎn)給藥毒性試驗應在兩種性別的動物上進行。人類、恒河猴和兔的眼軸長度存在性(xìng)別(bié)差異,但眼球(qiú)尺寸的性別差異卻極其微小(xiǎo)。Wagner等人(2008)研究了健康人眼和患病人眼的性別差異,認為性激素影響了不(bú)同性別在患病狀態下的淚腺係統、眼瞼和眨眼頻率、以及角膜的解剖和特征。一般(bān)而言,幹眼流行病學(xué)研究(jiū)表明女性幹眼發病率比男性高。然而,實驗動物(wù)的眼睛是否存在顯著的性別差(chà)異尚不明確。是(shì)否在(zài)滴眼給藥毒性試驗中(zhōng)使用兩(liǎng)種性別,尤其僅進行眼毒性評估的試驗,仍有待進一(yī)步討論。
03、給藥
劑量和濃度
根據ICH M3指導原則(ICH,2009),一般毒性試驗的高劑量水平設(shè)定為最大(dà)耐受量(MTD)、最(zuì)大給藥量(MFD)或人體暴露量的50倍。這一設定原(yuán)則同樣適用(yòng)於滴眼(yǎn)給藥毒(dú)性(xìng)試驗。在某(mǒu)些情況下,高劑量水平可以基於局部耐受性預試驗(yàn)的結果(guǒ)來確定。然而,在大多數情況下,滴眼給藥毒性試驗的高劑量水平是根據MFD設(shè)定(dìng)的(de),主要是由於製劑製備的某些(xiē)內在因(yīn)素。
供試品的角膜滲透性主要取決於製(zhì)劑的特性。為了獲得有意義的風險評估結果(guǒ),權威性(xìng)滴眼給藥毒(dú)性試驗(例如首次人體試驗之前開展的GLP試驗)所用的供試製劑應與(yǔ)臨床試(shì)驗(yàn)所用的製劑一致或相近。供試品的濃度主要是根據(jù)其(qí)在製劑(jì)中(zhōng)的溶解度來定(dìng)義的。至於製劑的調整(zhěng),其他特性(如滲透壓、pH值(zhí)和賦形劑)也十(shí)分重要。滴眼液製劑的(de)酸堿度應在可接受的生理範圍內。選擇防腐劑時,需避免其濃度達到引起毒性反應(yīng)的水平。例如,有研究者發現(xiàn),眼科製劑(jì)中常用的防腐劑苯紮氯銨在局部給藥時會誘發角膜變化。因此,眼科(kē)製劑中防腐劑的濃(nóng)度是有限製的。因此,在大多數情況下,滴眼給藥毒性試驗所設的最高劑量水平是基於受試製劑的最大給藥量,而非(fēi)供試品本(běn)身的特性(xìng)來決定的。
滴眼體積
兔(tù)子的眼瞼較為鬆弛,結膜囊較大,因此能容(róng)納較大的滴眼液(yè)體(tǐ)積。根據OECD眼刺激試驗指導原(yuán)則,兔子的滴眼體積為0.1 mL(OECD, 2012)。該體積約為臨床標(biāo)準滴眼液用藥體積(約0.04 mL)的兩倍。從經(jīng)驗來看,不同物種的最大滴眼體積並不(bú)相同。例如,比格犬(quǎn)和兔子的最大可行體積相似,而食蟹猴的最大可行體(tǐ)積(jī)則是比格犬和兔子的兩倍多。
需注意(yì)的是,眼部暴露量並不會隨著滴眼體積的增(zēng)加而成比例增加,因為部(bù)分多餘的液(yè)體會通過鼻淚管流失。Lambert等(1993)假定在眼刺激(jī)試驗中,如果滴眼體積為0.01 mL(建議供試體積的十分之一),藥物與(yǔ)人眼刺激感受的相關性更佳。因此,滴眼給藥毒性試驗的(de)滴(dī)眼體積可能需進一步討論。增加(jiā)滴眼體積並不能(néng)有效提高眼(yǎn)部暴露量,反而可能導(dǎo)致係統暴露量增加,甚至引發(fā)意料之外的係統毒性反(fǎn)應。
單眼/雙眼給藥
供試品是(shì)單眼給藥還是雙眼給藥需慎重考慮。從動(dòng)物福利的角度出(chū)發,若無特殊原因(yīn),應將供試品滴入單側(cè)眼睛。如一隻眼給予供試(shì)品,另一(yī)隻眼則不給藥(即不(bú)接觸供試品),或給予對照品(例如溶媒製劑)作(zuò)為對照。然而(ér),嚴格來說,對照眼由於係統循環的影(yǐng)響,可能也會接觸(chù)到(dào)供試品。因此,在評估對照眼的結果(guǒ)時,應該考慮到這一潛在的接觸因素。
給藥頻率(lǜ)
在標準的口服或靜脈給藥一般(bān)毒性試驗中,通常每(měi)天給藥一次;而在滴眼給藥毒性試驗中,通常一(yī)天給藥多次。非臨床試驗的滴眼頻(pín)率通常高於臨床(chuáng)試驗的給藥頻率。例如,非臨床試驗中可能(néng)每天滴眼4次,而(ér)臨床試驗(yàn)中則每天滴眼2次。滴(dī)眼給藥毒性(xìng)試驗設定較(jiào)高(gāo)的給藥頻率,旨在獲得更(gèng)高的重複暴露量,特(tè)別(bié)是在供(gòng)試品的生化特征導(dǎo)致最大藥物濃(nóng)度難以(yǐ)增加時更(gèng)為重要。Chrai等人(1974)報告稱,如果兩次滴眼間隔5分鍾,就能有效地增(zēng)加(jiā)兔(tù)的眼部暴露量。許多滴眼給藥(yào)毒性試驗的給藥頻率(lǜ)是臨床給藥頻(pín)率的1.5到2倍(bèi)。然而,給藥過於頻繁(fán)雖可提高暴露水平,但也增加操(cāo)作的次數,從而增加動物(wù)保定的頻率,這可能導致動物應激,進而引發倫理(lǐ)問(wèn)題(tí)。因此,在設計(jì)滴眼給藥毒性試驗時(shí),需在提高暴露水(shuǐ)平和減(jiǎn)少動物應激之間找到平衡(héng)點,以確保試驗的科學性和倫(lún)理性。
04、眼及附屬組織檢查
常規/標準眼科學(xué)檢(jiǎn)查
滴眼給藥毒性試驗目前尚無統一(yī)的眼部和係統檢查(chá)項目(mù)。OITSs的眼科學檢查是基於係統藥物一般毒性(xìng)評估指導原則進行的,涵(hán)蓋了眼前節、眼(yǎn)內介質和(hé)眼底等所有組織的檢查(ICH, 1999)。然而,由於滴眼給藥直接(jiē)作(zuò)用於眼部,滴眼給藥毒性試驗的眼科學檢(jiǎn)查更(gèng)加詳細,涵蓋(gài)的檢查項目也更多。Weir和(hé)Wilson(2013)列(liè)出了非臨(lín)床眼毒性(xìng)試驗的標準眼部(bù)安全性終(zhōng)點,這些終點具有重要的借鑒意義。檢查項目包括:大(dà)體觀察(chá)、裂隙燈生物顯微鏡檢查、眼底檢(jiǎn)眼鏡檢(jiǎn)查、眼壓測量、視網膜電圖和組織病理學。
基於相關指導原則和知識,表3總結了滴(dī)眼給藥毒性試驗(yàn)的常規及可選眼科檢查項目。由於眼前節的供試品濃度較高,因此對眼前節進行觀察和檢查尤為重要。除標準的大體觀察外,采用(yòng)評分方法(fǎ)進行(háng)詳細觀(guān)察對於評估(gū)眼毒性(xìng)的嚴重程度非常關鍵。例如,Draize評分法用於角膜、虹膜和結膜的大體觀(guān)察。McDonald Schadduck評分和Hackett-McDonald評分常應用於(yú)滴(dī)眼給藥毒性試驗中,二者對裂隙燈顯微鏡檢(jiǎn)查結果進行評分。特別是,Hackett-McDonald評分能對眼睛進行全麵評(píng)估,包括對晶體和瞳孔光反射的評估(gū)。
表3 滴眼給藥毒性試驗的常規或可選眼科(kē)學(xué)檢查
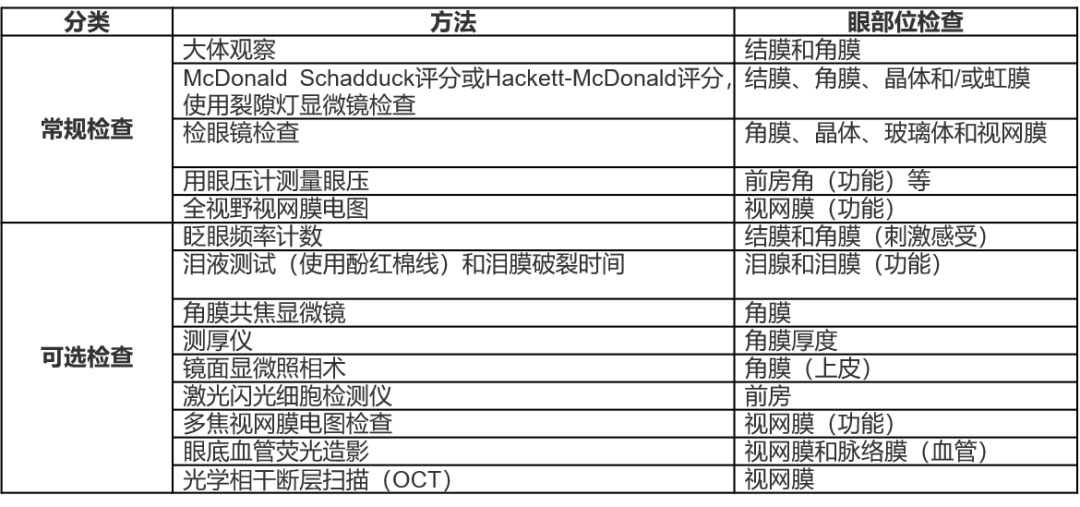
常規檢查包括利用檢眼鏡對玻(bō)璃體(tǐ)和眼(yǎn)底(dǐ)進行(háng)觀(guān)察。使用直接檢眼(yǎn)鏡(jìng)和(hé)間接檢眼鏡(jìng)可詳細檢查眼底。本(běn)原則建議,除拍照外,還應簡述檢查結果並記錄,並將這些記錄與相應的詳細記錄一同保存。
眼(yǎn)壓是衡量前(qián)房角功能變化的重要參數(shù)。FDA指導原則提到了使用(yòng)眼壓計的方法(FDA/CDER,2008)。在非臨床毒性試驗中,常用(yòng)扁平眼壓計、回彈式眼壓計或空氣式(shì)眼壓計(jì)來測量眼壓。在滴眼(yǎn)給藥毒性試驗中(zhōng),使用(yòng)眼壓計有幾點注意事項。首(shǒu)先,為了獲得準確的眼壓值,有必要使動物適應眼壓計。在測量之前,如果動物沒有適應(yīng)眼壓(yā)計,通常情(qíng)況下測出的眼壓值(zhí)會偏高,從(cóng)而導致無法正確(què)判斷藥效。其次,由於(yú)儀器會接觸(chù)角膜表麵,眼(yǎn)壓測量操作可能會在某種程度上損傷角膜上皮細胞。因此,應慎重決定檢查的組別及檢查順(shùn)序,以(yǐ)避免眼部過度應激,並防(fáng)止過度應激影響(xiǎng)其他結果的解(jiě)讀。
通過全視野視網膜電(diàn)圖檢查(chá)(ffERG)可檢測視網膜(mó)的功能變化。理想的做法是使用國際臨床視(shì)覺電生理協(xié)會(ISCEV)建議的方法,因為(wéi)此方(fāng)法可在進(jìn)行全視野視網膜電圖(tú)檢查時識(shí)別(bié)視錐細胞和視杆細胞的變化。然而(ér),此方法不適用於在有限時間內對大量動物進行檢查的情況。ISCEV方法擬用於隨診檢查(chá),可能僅適用於ERG檢查發現異常的情況。例如,Penha等人(2010)報告稱,角膜混濁或晶體混濁會影響光線到達視網膜,而麻醉也(yě)會影響全視野視網膜電(diàn)圖的檢查結果。
可選檢查
關於淚膜檢查(chá),Schirmer試驗和酚紅線(xiàn)試(shì)驗用於淚液體積的定量分析。進行Schirmer試驗和酚紅線試驗時,分別使用無毒濾紙或棉線浸潤於pH指(zhǐ)示劑酚紅溶液中,然後(hòu)插入結膜囊(náng)內進行淚膜(mó)檢測。淚膜的(de)其他臨床檢查包(bāo)括淚膜破裂時間。此前已有研究者報告了犬和兔的淚膜破裂(liè)時間,這些(xiē)測(cè)試(shì)能夠揭示(shì)淚腺的功能狀態。此外,眨眼頻率也可以間接說明(míng)供(gòng)試品是否對角膜產生了刺激。
由於眼科成像技(jì)術的(de)進步,現在能檢測出常(cháng)規眼科學檢查難以察覺的變化。例如,角膜(mó)共焦顯微鏡檢查能夠捕捉到(dào)角膜上皮(pí)的細微變化;角膜內皮顯微鏡檢查(chá)能(néng)夠觀察到角(jiǎo)膜內皮的(de)形態和密度變化;光學相幹斷層掃描(OCT)對於視網膜的觀察非常有力。這些成像技術(shù)均可用於滴(dī)眼給藥毒性試驗中的動物檢查,能夠生(shēng)成高分辨率的圖像,滿足組(zǔ)織病理學檢查的要(yào)求。
滴眼給藥毒(dú)性試驗的(de)其他常用眼前節檢查包括定量測量角膜厚度的測厚儀和定量測量前房房水閃輝的激光房(fáng)水閃光細胞儀。如果眼後節的視網膜(mó)出現局部異常,多焦視(shì)網膜(mó)電圖(mfERG)能(néng)夠捕捉到(dào)相應的電生理信(xìn)號。利用眼底血管熒光造影能夠觀察到視網膜和脈絡膜的原有血管及新生血管的滲透性。
Kontadakis等人(2014)指出(chū),淚膜中的細胞因子和生長因子作(zuò)為生物標記物,能預(yù)示眼表疾(jí)病。有(yǒu)研究者報告稱,血清細胞因子是預示老年黃斑變性的生物標記物。生物標記物能用於非侵(qīn)入性方式觀察藥物誘導的眼毒性反應。然而,目前(qián)這樣的生物標記物數量仍然有限。反過來,上述的各種眼部成像(xiàng)技術可能可替代生物標記物,用於觀察和研究人和動物的眼毒性。
05、眼及附(fù)屬(shǔ)組織(zhī)的病理(lǐ)學檢查
組織病理檢查是滴眼給藥毒性試驗的重要組成部分。最近,多篇文(wén)獻綜述一致強(qiáng)調了組織病理學檢查在藥物評(píng)估中的重要性。在滴(dī)眼給藥(yào)毒性試驗中,供試品的最大暴露量不僅出現在角膜上皮,還(hái)出(chū)現在結膜和排泄係統,包括鼻(bí)淚(lèi)管的粘膜和鼻腔。因此,需要特別注意細致檢查這些(xiē)組織。淚腺、哈氏腺(xiàn)(若有)、鼻腔和瞬膜(若有)也應進行組織病理學檢查。為了準確地進行組織病理學評估分析,必須嚴格考量組織病理切片的質量。如今已有(yǒu)多篇關於這(zhè)一方麵的文章發表,詳細闡述了(le)切片的各(gè)種技術考量。


